成果简介
近日,武汉大学土木建筑工程学院黄理志团队在环境领域著名学术期刊Water Research上发表了题为“Mineralization of tribromophenol under anoxic/oxic conditions in the presence of copper(II) doped green rust: Importance of sequential reduction-oxidation process”的论文。文中研究了无氧/有氧/无氧-有氧环境下三溴苯酚(TBP)在绿锈(GR)和金属离子Cu(II)存在下的降解。在无氧条件下,GR-Cu(II)在7h内将TBP完全还原为4-BP,在有氧条件下,GR-Cu(II)通过活化分子氧生成?OH氧化降解TBP,但单一还原或氧化作用均无法实现TBP的矿化。通过连续还原-氧化过程可实现65% 的TBP矿化,说明GR-Cu(II)的存在极大地影响了TBP在无氧/有氧-交替地下水环境中的命运,GR-Cu(II)对TBP的连续还原-氧化降解是未来TBP污染的地下水修复的一种有前景的方法。
引言
GR是无氧地下水环境中的含有Fe(II)和Fe(III)的铁氢氧化物,Cu是地下环境中相对丰富的微量金属。Cu可以吸附在环境相关的Fe(III)(氢氧)氧化物上,它们在还原性地下环境下的还原性溶解可能导致GR的形成和Cu(II)的同时释放。由于原电池效应,Cu(II)的存在显著提高了GR的还原反应性。Cu掺杂GR在无氧条件下能够加速各种有机污染物的还原转化。然而,即使一些有机污染物如卤代芳烃(HAHs)的完全还原产物,仍然是有毒的。研究表明顺序还原-氧化过程对HAHs完全矿化有效,因为还原过程中形成的芳烃可以在后续的氧化过程中得到有效降解。然而先前关于两阶段还原/氧化法的研究中使用的材料大多是合成纳米材料,而不是自然形成的材料,在本研究采用的Cu(II)掺杂GR(GR-Cu(II))与环境高度相关。同时,地下水环境往往由于自然过程或人类活动会发生从无氧到有氧的转变,这为HAHs可能的连续还原-氧化降解提供了自然发生的条件。以往对GR或GR-Cu(II)的研究仅限于单一的无氧或有氧环境。在本研究中,我们探索了在地下环境中,TBP在无氧-有氧边界被GR-Cu(II)顺序还原-氧化降解进而矿化的可能性。本文首次研究了TBP与GR-Cu(II)在无氧、有氧及无氧-有氧三种不同环境条件下的相互作用。此外,通过自由基猝灭实验、中间产物分析和密度泛函理论(DFT)计算,揭示了TBP的还原和氧化降解途径。
图文导读
无氧条件下TBP的还原
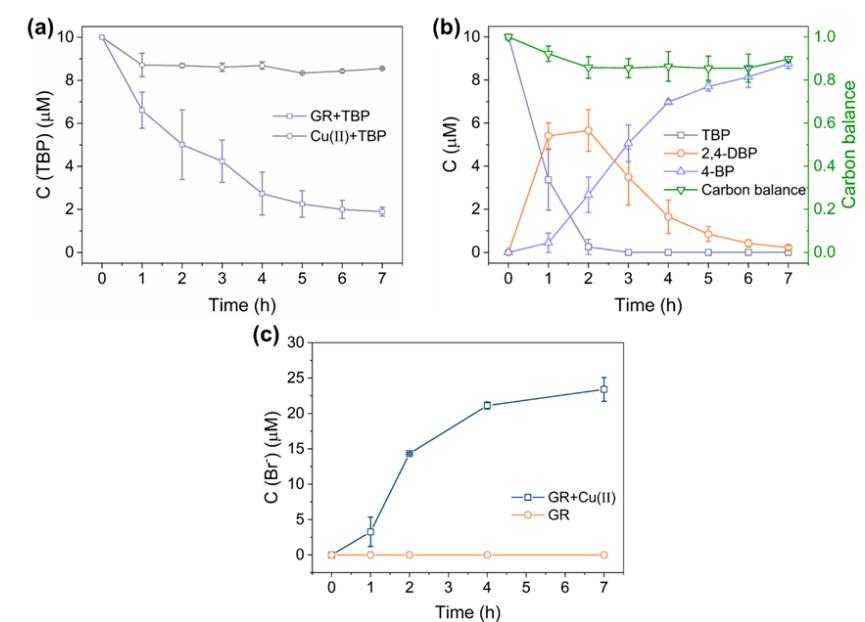
图1:(a)单独GR或Cu(II)与TBP的作用效果,(b)GR-Cu(II)对TBP的还原降解,(c)在无氧条件下GR和GR-Cu(II)与TBP作用过程中产生的Br–。
Cu(II)对TBP无还原作用,反应7小时后,约80%的TBP被GR去除,但未检测到降解产物(图1a),表明TBP的去除是由于GR的吸附。相比之下,TBP在3h内被GR-Cu(II)完全还原并经历了一个连续的脱溴过程(TBP→2,4-DBP→4-BP),最终在7h后还原降解为4-BP(图1b),同时约20?M的Br–被释放到反应溶液中(图1c)。
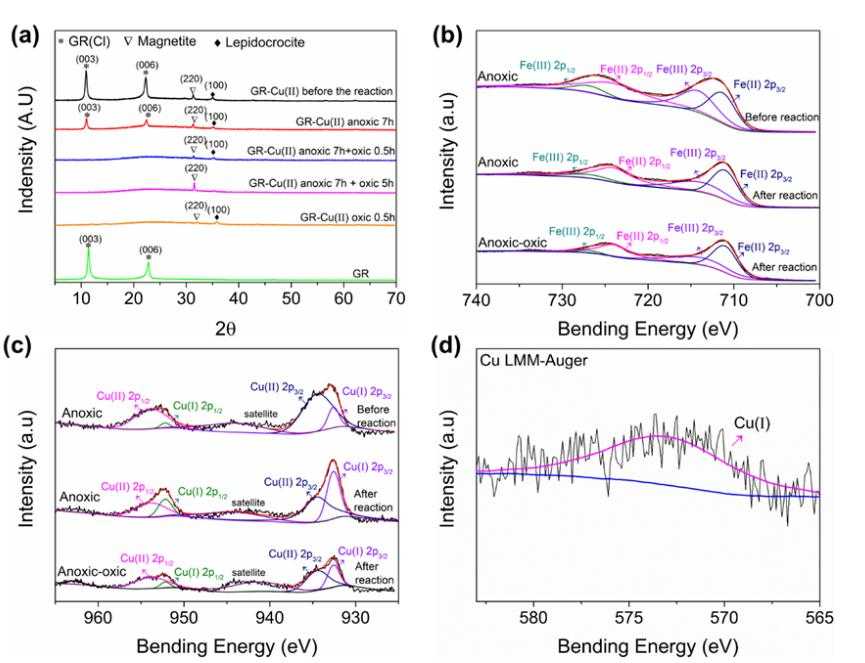
图2:在不同反应条件下GR-Cu(II)的(a)XRD谱图,(b) Fe 2p XPS和(c) Cu 2p XPS,(d)在无氧条件下与TBP相互作用之前GR-Cu(II)的Cu LMM俄歇光谱。
GR-Cu(II)与TBP反应前后的XRD谱图如图2a所示。Cu(II)的加入导致GR部分转化为纤铁矿和磁铁矿。GR-Cu(II)与TBP在缺氧条件下反应7小时后,GR特征峰的强度明显减弱。通过XPS分析确定了Cu和Fe物种(图2b-d),证实了GR将Cu(II)还原为Cu(I)。无氧反应7 h后仍可检测到Cu(I)(图2c),表明Cu(I)在还原TBP的过程中是充足的。
TBP在有氧条件下的氧化降解
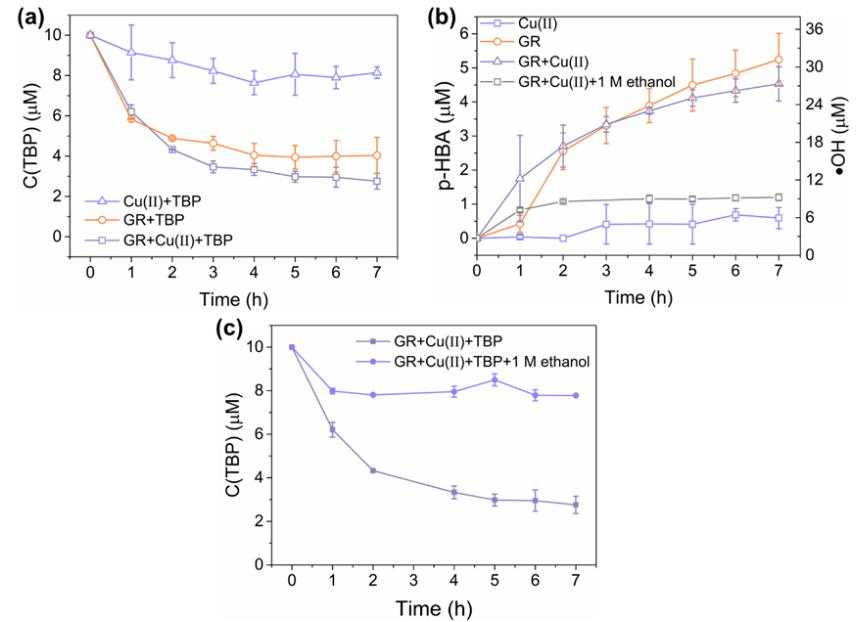
图3:(a)有氧条件下GR-Cu(II)对TBP的降解,(b)GR-Cu(II)氧化过程中的累积?OH的浓度,(c)有氧条件下的?OH猝灭实验。
氧化7小时后,GR单独去除TBP的效率达到60%,GR-Cu(II)对TBP的去除率提高到73%(图3a)。使用苯甲酸(BA)羟基化为对羟基苯甲酸(p-HBA)作为探针反应,对GR和GR-Cu(II)氧化产生的?OH累积浓度进行定量(图3b)。GR和GR-Cu(II)逐渐产生30?M左右的?OH。相比之下,添加1M乙醇后,TBP的降解被显著抑制(图3c),这表明?OH是GR-Cu(II)氧化降解TBP的原因。Cu(I)和Fe(II)都能够还原O2,但Cu(I)还原O2的活性高于Fe(II)。所以 GR-Cu(II)在早期产生?OH的速率高于GR,而后期Cu(I)被消耗,其重新产生速率缓慢,?OH生成的速率下降。
无氧-有氧转化条件下TBP的矿化
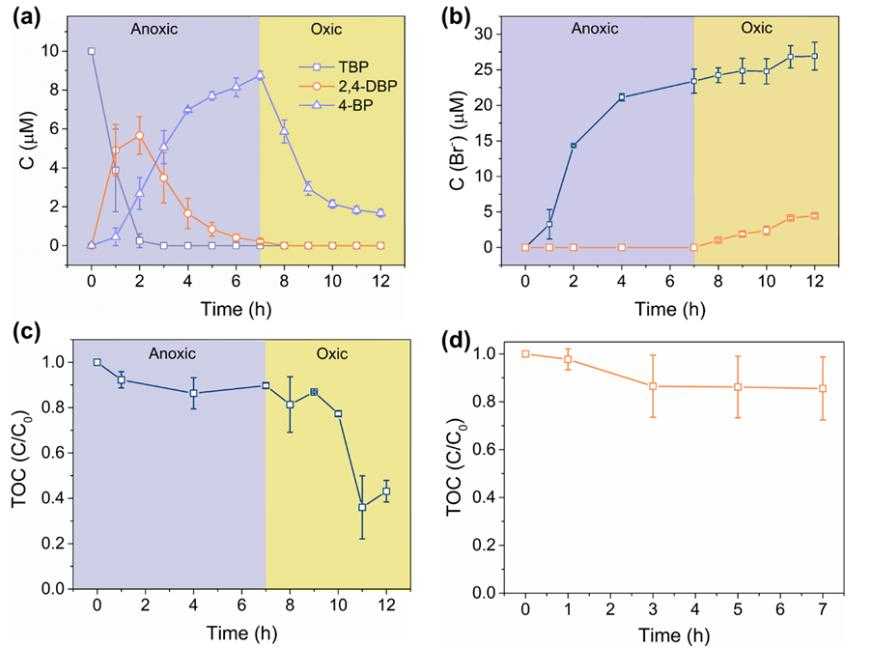
图4:(a)TBP在无氧-有氧转化条件下的降解及(b)Br–的释放, (c)TBP在无氧-有氧转化条件下及(d)单独有氧条件下TOC的变化
GR-Cu(II)在无氧条件下将TBP完全还原为4-BP,约81%的4-BP在无氧到有氧转化后5小时内被降解(图4a)。反应溶液中释放的Br?逐渐增加至26.9?M(图4b)。GR在无氧过程中不产生Br?,而在氧化过程中只产生4.4μM的Br?。此外,GR-Cu(II)在单一有氧环境下仅检测到10μM左右的Br?,说明TBP在无氧条件下的还原脱溴过程是后续氧化降解所必需的。4-BP不能在无氧条件下继续降解,表明在氧条件下生成?OH对4-BP的进一步降解是必要的。在无氧条件下TOC基本保持在90%,但在随后的有氧条件下显著下降到35%(图4c)。推测TBP的羟基化/苯环断裂是在氧化条件下发生的,之后生成的有机片段会进一步氧化降解。TBP通过顺序还原-氧化脱溴实现约65%的矿化,而TOC值在单一有氧条件下几乎没有变化(图4d)。因此,还原氧化作用相结合是GR-Cu(II)对TBP矿化的有效途径。
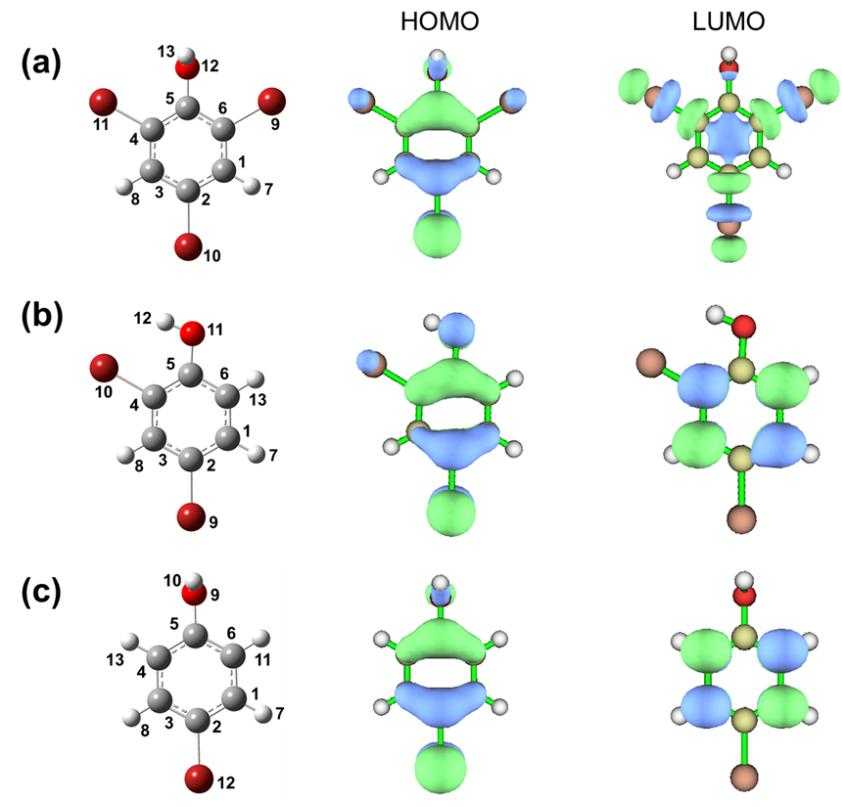
图5:(a)TBP,(b) 2,4-DBP和(c) 4-BP的化学结构、LUMO和HOMO。
利用DFT计算进一步阐明降解途径(图5)。TBP的LUMO主要集中在C-Br键上。因此,这些位点容易获得电子,从而导致TBP的还原脱溴。此外,从图中可以看出,HOMO轨道主要围绕在TBP和4-BP的富电子原子Br10和Br12周围。?OH是一种亲电物种,可以引起自由基攻击。因此,TBP的Br10和4-BP的Br12是主要的羟基化反应位点,形成2,6-二溴对苯醌和对苯二酚。
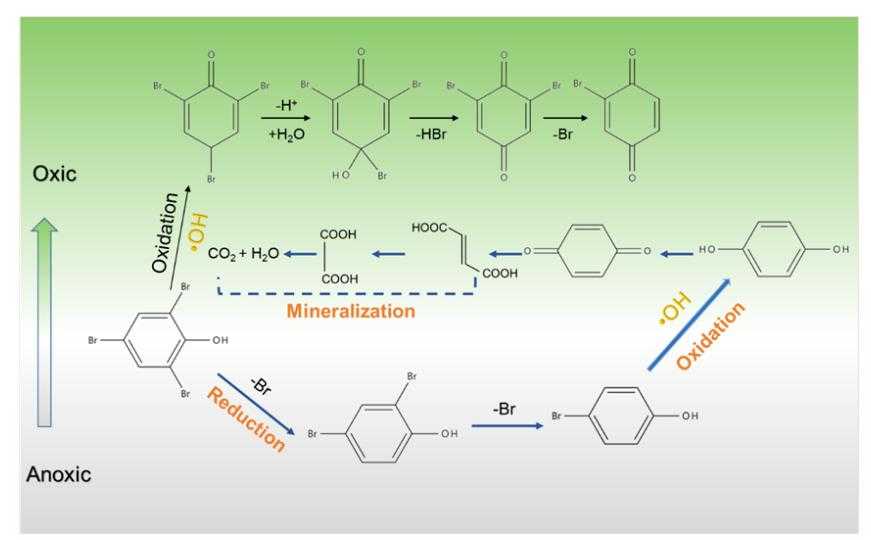
图6:GR-Cu(II)在无氧、有氧和无氧-有氧转化条件下的TBP降解途径。
根据HPLC-MS数据和DFT计算,提出了在三种不同环境下TBP可能的降解途径(图6)。在无氧条件下,TBP可被GR-Cu(II)还原脱溴生成4-BP。在有氧条件下,TBP的C-Br10键在?OH的作用下断裂,形成2,6-二溴对苯醌,进一步降解为2-溴-1,4-苯醌。在无氧到有氧的转变过程中,无氧阶段TBP还原为4-BP导致苯环上电子云密度增加,这有利于后续有氧阶段4-BP的?OH攻击和苯环打开过程。4-BP的Br12首先被羟基化,然后?OH对多羟基化合物产物进一步攻击而发生开环反应。随后,产生短链羧酸,它们被?OH进一步氧化成CO2和H2O。观察到TBP在单独还原或氧化过程中未完全脱溴,其产物仍有毒性。因此,还原和氧化的结合对于TBP的完全解毒是更好的方法。
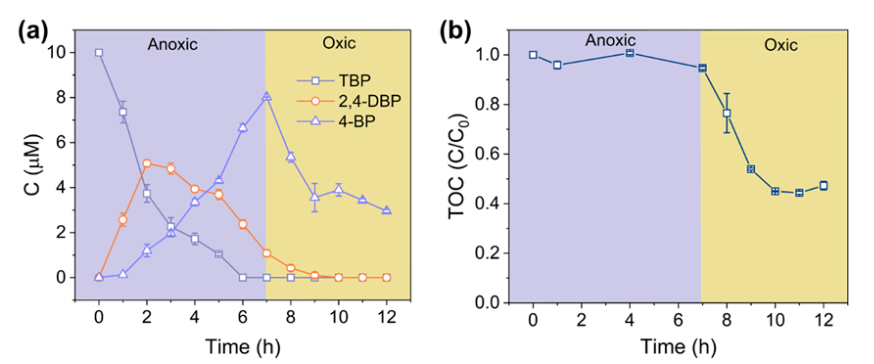
图7:在无氧-有氧转化条件下,GR-Cu(II)在实际地下水中对TBP的(a)降解和(b)矿化
使用实际地下水作为实验用水,GR-Cu(II)对TBP的连续还原和氧化作用仍可发生,同时也实现了TBP的矿化(图7)。TBP去除速率略有下降,最终矿化效率为55%。低于超纯水中的65%。地下水中的SO42-可能与竞争GR-Cu(II)的反应位点,从而抑制GR-Cu(II)对TBP的降解。
小结
本研究发现Cu(II)的存在增强了GR在无氧条件下对TBP的还原反应性,将TBP去除机制从吸附改变为还原脱卤。TBP在7 h内被GR-Cu(II)还原为4-BP。GR和GR-Cu(II)在有氧条件下都能活化分子氧产生·OH,导致TBP的氧化降解。Cu(II)的存在增加了GR氧化过程中最初2 h内?OH的产生速率,但略微降低了?OH的最终累积浓度。在无氧条件下的还原脱卤产物4-BP可以在随后的有氧条件下被GR-Cu(II)进一步降解。GR-Cu(II)在连续的还原-氧化过程中实现了TBP的完全降解和65%的矿化,这表明GR-Cu(II)可以在无氧/有氧交替的地下环境中有效地降解TBP。这项工作全面探究了无氧、有氧和无氧到有氧条件下TBP和GR-Cu(II)之间的相互作用,突出了还原和氧化结合过程对TBP矿化的作用。